Per le lesioni più ampie
prf - Platelet Rich Fibrin
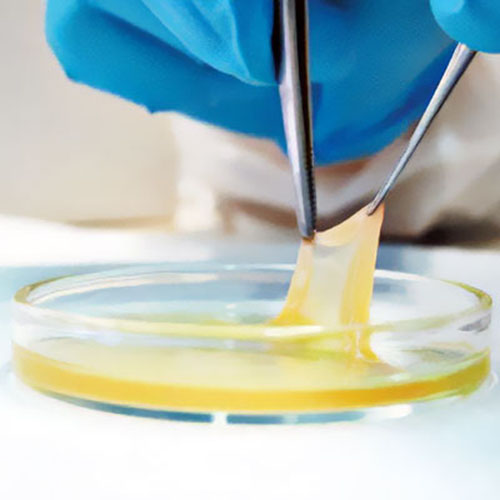
plastico, elastico e di facile manipolazione
Quando le dimensioni contano
La soluzione in questi casi è il PRF (Platelet Rich Fibrin), un concentrato piastrinico di 2° generazione con struttura simile a quelle del CGF, anche se di minore densità.[1,17,18] che può essere ottenuto, usando specifici protocolli, sotto forma di membrane gel fino a 6-9 cm di diametro, Ciò lo rende ideale per un uso come agente di copertura nelle lesioni più ampie, in perfetta sinergia con il suo “fratello maggiore” CGF , dove la membrana PRF può coprire e stimolare le zone periferiche della lesione mentre il CGF, più concentrato, si occupa delle zone più difficili.
Il PRF (Platelet-Rich-Fibrin) è un concentrato piastrinico di 2° generazione (laddove la 1° è rappresentata dal PRP e la 3° dal CGF,)[1]che si ottiene centrifugando sangue intero in provette prive di anticoagulante (o nelle quali l’anticoagulante è stato neutralizzato). Esistono numerosi protocolli per la preparazione, a cominciare (L-PRF) creato dal francese Choukroun nel 2001.
Da allora, particolarmente dopo lo sviluppo del CGF da parte di Sacco nel 2006, si sono susseguite almeno una decina di altre formulazioni di PRF, molte delle quali create dopo il 2014 dell’americano Miron.

Sotto: Membrana PRF ottenuta da una singola provetta
Indiscutibile efficacia clinica
Il PRF contiene - sebbene ad una concentrazione minore - gli stessi fattori di crescita del CGF - PDGF, TGF-b,IGF, EGF, FGF, BMP e VEGF.: Non bisogna quindi assolutamente pensare al PRF come ad un emocomponente di serie B: oltre un decennio di letteratura clinica che ne dimostra l'efficacia nella riparazione dei tessuti molli, superata solo da quella del CGF – in media l’87% degli studi riporta effetti benefici dall'uso del PRF nella rigenerazione dei tessuti molli e nel wound healing.[9] Alcuni esempi:
- Riduzione di dimensioni della lesione in 287 su 288 casi di lesioni croniche di varia eziologia refrattarie alla terapie tradizionali trattate settimanalmente con PRF; completa risoluzione nell’ 81% dei casi trattati per almeno 6 settimane. Tutte le DFU e tutte le VLU ≤ 10cmq sono guarite completamente entro 3 mesi.[7 rif.45,]
- Una sola recidiva su 107 casi a 6 -12 mesi dopo trattamento con PRF. Tutti i casi hanno riportato riduzione di dolore, odori, ed infezioni già dopo 2-3 settimane. [7 rif.44,47-50].
- Dimostrata riduzione di infezioni postoperatorie, necrosi dell’innesto, recidive e necessità di amputazione [7 rif.57].
- Dimostrata superiorità alle terapie tradizionali nelle VLU,con una maggiore riduzione di dimensioni della lesione a 4 settimane (-86% vs 43% a 4 settimane, 100% vs 62% ad 8 settimane) [7 rif.69,72].
- Versatilità ed efficacia dimostrate in numerosi piccoli studi su ulcere trofiche, Pyoderma gangrenosum, DFU con osteomielite, fistole uretrali, perforazioni timpaniche, ricostruzioni ossee del cranio, rimozioni parotidee, e copertura dei siti donatori per trapianti cutanei. [7 rif.66-72]
- Chiusura di una vasta deiscenza addominale con fuoriuscita di organi, infetta da Klebsiella e Candida, in sole 9 settimane; chiusura di una lesione traumatica con tibia e tendini esposti in 10 settimane; Guarigione di una ampia lesione ischemica al piede in 10 settimane [7].
- Risultati eccellenti sulle DFU (Crisci) [3,rif.23]
- Accelerazione della guarigione e riduzione del dolore nei siti di prelievo degli innesti cutanei nei pazienti ustionati [3, rif.24].
- Efficacia nelle ferite croniche ampiamente superiore alle medicazioni tradizionali, quali garza paraffinata[7 rif.46], garze imbevute di fisiologica[7 rif.52] ed unguenti caricati con EGF ricombinante.[7 rif.56]
- Aumento della creazione di tessuto di granulazione, e riduzione di dimensioni della lesione fin dalla prima applicazione su lesioni croniche recalcitranti e stagnanti in media da 1 anno ,di cui almeno la metà arrivata a chiusura prima della 5°applicazione.[10]
- In uno studio multicentrico su 44 pazienti, perlopiù VLU e DFU nelle quali le terapie rtadizionali avevano fallito, il PRF ha portato a chiusura la totalità delle lesioni sotto i 10 cmq in media entro 9 settimane ed il 75% di quelle di dimensioni superiori, in media entro una quindicina di applicazioni. [11]
Nato Per L'Utilizzo Combinato
Il PRF è stato infatti usato fin dall’inizio in combinazione con osso autologo o eterologo disidratato con eccellenti risultati nella ricostruzione di difetti ossei.[02] .
E' stato poi usato con successo per imbibire scaffolds per rigenerazione guidata[17,24], o in combinazione con staminali da tessuto adiposo (HADSCs)[03] o ancora in combinazione con acido ialuronico[07].
La sua azione antibatterica[03], dovuta ai leucociti intrappolati nella matrice fibrinica[18], è stata sperimentalmente potenziata addizionando al sangue prelevato vari mix di antibiotici[14,17] con risultati apparentemente molto positivi[01,14], ma c’è discussione in merito alla dose di antibiotico da addizionare: se troppo alta rischia di inficiare le caratteristiche fisiche del PRF[1] o rilasciare una dose tossica iniziale ed una dose insufficiente nei giorni successivi.[17]

Un Protocollo di Produzione Specifico
I kit High Q Cell All-In-One e Patch Plus contengono infatti, oltre a provette a tappo rosso per la produzione di CGF, anche provette a tappo blu, con gel separatore, per la produzione di PRP.
Il protocollo utilizzato da High Q Cell per la produzione di patch piastrino-fibriniche di PRF di ampie dimensioni prevede il recupero, tramite siringa ed ago spinale in dotazione, del liquido sovranatante ricco di trombina che si libera nelle provette per la produzione del CGF (tappo rosso) durante il distacco del coagulo dalla parete della provetta.
Il sovranatante recuperato viene poi aggiunto al PRP ottenuto dalle centrifugazione dei campioni raccolti nelle provette per la produzione di PRP (tappo blu) depositato in una piastra Petri sterile da 60 o 90mm per attivarne la coagulazione.
Dopo qualche minuto - tenendo presente che per una valida coagulazione di 10cc di PRP occorre almeno 1 cc di trombina autologa (rapporto Trombina:PRP ≥ 1:10) - il PRP contenuto nella Petri gelifica formando una membrana PRF.
Tale membrana può essere prelevata con una spatola sterile ed utilizzata a copertura della lesione e degli eventuali coaguli CGF già applicati nelle zone più problematiche della lesione stessa, coprendo poi il tutto con una medicazione primaria.
Bibliografia
- [01] Salgado-Peralvo AO, Kewalramani N, et al: Understanding Solid-Based Platelet-Rich Fibrin Matrices in Oral and Maxillofacial Surgery: An Integrative Review of the Critical Protocol Factors and Their Influence on the Final Product. Medicina 2023, 59, 1903. https://doi.org/10.3390/medicina59111903
- [02] Grecu AF, Reclaru L, et al: Platelet-Rich Fibrin and Its Emerging Therapeutic Benefits for Musculoskeletal Injury Treatment. Medicina 2019, 55, 141; https://doi.org/10.3390/medicina55050141
- [03] Wu QY, Zhang Q, et al : Clinical Application of Platelet-Rich Fibrin in Dermatology, Int J of Dermatology and Venereology (2022) 5:3. https://doi.org/10.1097/JD9.0000000000000186
- [04] Miron RJ, Fujioka-Kobayashi M, et al: Optimization of platelet-rich fibrin. Periodontology 2000. 2024;94:79-91. https://doi.org/10.1111/prd.12521
- [05] Farshidfar N, Amiri MA, et al.: Platelet-rich plasma (PRP) versus injectable platelet-rich fibrin (i-PRF): A systematic review across all fields of medicine. Periodontology 2000. 2025;00:1-3. https://doi.org/10.1111/prd.12626
- [06] Choukroun J, Ghanaati S: Reduction of relative centrifugation force within injectable platelet-rich-fibrin (PRF) concentrates advances patients’ own inflammatory cells, platelets and growth factors: the first introduction to the low speed centrifugation concept. Eur J Trauma Emerg Surg (2018) 44:87–95. https://doi.org/10.1007/s00068-017-0767-9
- [07] Pinto N, Yu J, et al: L-PRF in extra-oral wound care. Periodontology 2000. 2025;97:342-362. https://doi.org/10.1111/prd.12605
- [08] Miron, RJ, Tomoyuki K, et al: A technical note on contamination from PRF tubes containing silica and silicone. BMC Oral Health (2021) 21:135. https://doi.org/10.1186/s12903-021-01497-0
- [09] Miron RJ, Fujioka-Kobayashi M, et al: Platelet-Rich Fibrin and Soft Tissue Wound Healing: A Systematic Review. Tissue Engineering B 23 : 1, 2016. https://doi.org/10.1089/ten.teb.2016.0233
- [10] Bilgen F, Ural A, et al: Platelet-Rich Fibrin: An Effective Chronic Wound Healing Accelerator. Journal of Tissue Viability, 4:009. https://doi.org/10.1016/j.jtv.2021.04.009
- [11] Pinto NR, Ubilla M, et al: Leucocyte- and platelet-rich fibrin (L-PRF) as a regenerative medicine strategy for the treatment of refractory leg ulcers: a prospective cohort study. Platelets (2017). http://dx.doi.org/10.1080/09537104.2017.1327654
- [12] À-João Abel Sá-Oliveira JA, Vieira Geraldo M, et al: Bioactivity of dressings based on platelet-rich plasma and Platelet- rich fibrin for tissue regeneration in animal model. World J Biol Chem. Mar 5, 2025; 16(1): 98515. https://doi.org/10.4331/wjbc.v16.i1.98515
- [13] Yuan Y, Xu B, et al: Effects of platelet-rich fibrin on post- extraction wound healing and wound pain: A meta-analysis. Int Wound J. 2024;21(2):e14654. https://doi.org/10.1111/iwj.14654
- [14] Miron RJ, Gruber R, et al: Ten years of injectable platelet-rich fibrin. Periodontology 2000. 2024;94:92-113. https://doi.org/10.1111/prd.12538
- [15] Zheng X, Yan X, et al: Exploration of proper heating protocol for injectable horizontal platelet-rich fibrin gel. Intl J Implant Dent (2022) 8:36. https://doi.org/10.1186/s40729-022-00436-0
- [16] Fujioka-Kobayashi M, Schaller B, et al: Biological characterization of an injectable platelet-rich fibrin mixture consisting of autologous albumin gel and liquid platelet-rich fibrin (Alb-PRF).Platelets (2020). https://doi.org/10.1080/09537104.2020.1717455
- [17] Egle K, Salma I, et al: From Blood to Regenerative Tissue: How Autologous Platelet-Rich Fibrin Can Be Combined with Other Materials to Ensure Controlled Drug and Growth Factor Release. Int. J. Mol.Sci.2021,22,11553. https://doi.org/10.3390/ijms222111553
- [18] Fujioka-Kobayashi M, Miron RJ, et al.: Optimized Platelet-Rich Fibrin With the Low-Speed Concept: Growth Factor Release, Biocompatibility, and Cellular Response. J Periodontol 2017;88:112-121. https://doi.org/10.1902/jop.2016.160443
- [19] Pavlovic,V, Ciric M, et al: Platelet-rich fibrin: Basics of biological actions and protocol modifications. Open Medicine 2021; 16: 446–454. https://doi.org/10.1515/med-2021-0259
- [20] Miron, RJ: Understanding PRF. Quintessence Publishing Blog, February 4,2021. https://www.quintpub.net/news/2021/02/understanding-prf/. Retrieved July,4, 2025.
- [21] Miron RJ, Chai J, et al: Evaluation of 24 protocols for the production of platelet-rich fibrin. BMC Oral Health (2020) 20:310. https://doi.org/10.1186/s12903-020-01299-w
- [22] Wei Y, Chong Y, et al.: Development of a super-hydrophilic anaerobic tube for the optimization of platelet-rich fibrin. Platelets, 35:1, 2316745. https://doi.org/10.1080/09537104.2024.2316745
- [23] Davies C, Miron RJ. Autolougous platelet concentrates in esthetics medicine. Periodontology 2000. 2025;97:363-419. https://doi.org/10.1111/prd.12582
- [24] Al-Maawi S, Herrera-Vizcaìno C, et al.: Biologization of Collagen-Based Biomaterials Using Liquid-Platelet-Rich Fibrin: New Insights into Clinically Applicable Tissue Engineering. Materials 2019, 12, 3993; https://doi.org/10.3390/ma12233993
- [25] Choukroun J, Adda F, et al: Une opportunité en paroimplantologie: le PRF. Implantodontie, 2001 ; 42 : p. 55–62.
